Содержание
Влияние катализатора на скорость химических реакций
Вещества,
которые участвуют в реакциях и увеличивают
ее скорость, оставаясь к концу реакции
неизменными, называются катализаторами.
Явление
изменения скорости реакции под действием
таких веществ называется катализом.
Реакции, протекающие под действием
катализаторов, называются каталитическими.
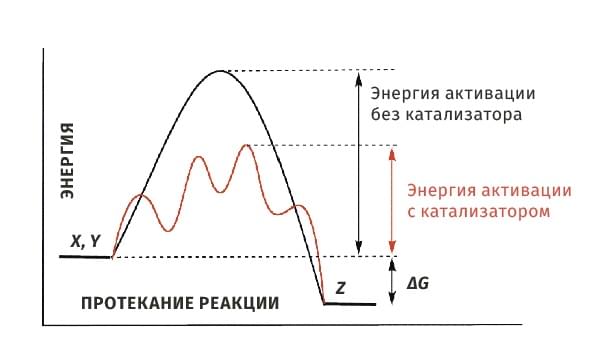
В
большинстве случаев действие катализатора
объясняется тем, что он снижает энергию
активации реакции. В присутствии
катализатора реакция проходит через
другие промежуточные стадии, чем без
него, причем эти стадии энергетически
более доступны. Иначе говоря, в присутствии
катализатора возникают другие
активированные комплексы, причем для
их образования требуется меньше энергии,
чем для образования активированных
комплексов, возникающих без катализатора.
Таким образом, энергия активации резко
понижается: некоторые молекулы, энергия
которых была недостаточна для активных
столкновений, теперь оказываются
активными.
Для
ряда реакций промежуточные соединения
изучены; как правило, они представляют
собою весьма активные нестойкие
продукты.
Механизм
действия катализаторов связан с
уменьшением энергии активации реакции
за счет образования промежуточных
соединений. Катализ можно представить
следующим образом:
А + К = А*
А*
+ В = С + D
+ К,
где
А*
— промежуточное активированное соединение.
В
химической промышленности катализаторы
применяются весьма широко. Под влиянием
катализаторов реакции могут ускоряться
в миллионы раз и более. В некоторых
случаях под действием катализаторов
могут возбуждаться такие реакции,
которые без них в данных условиях
практически не протекают.
Различают
гомогенный
и гетерогенный катализ.
В
случае гомогенного
катализа
катализатор и реагирующие вещества
образуют одну фазу (газ или раствор). В
случае гетерогенного
катализа
катализатор находится в системе в виде
самостоятельной фазы.
Примеры
гомогенного катализа:
1.
окисление SO2
+ 1/2O2
= SO3
в присутствии NO.
NO
легко окисляется до NO2,
а NO2
уже окисляет SO2;
2.
разложение пероксида водорода в водном
растворе на воду и кислород. Ионы Сг2О2=7,
WO2-4,
МоО2-4,
катализирующие разложение пероксида
водорода, образуют с ним промежуточные
соединения, которые далее распадаются
с выделением кислорода.
Гомогенный
катализ осуществляется через промежуточные
реакции с катализатором и в результате
происходит замена одной реакции с
высокой энергией активации, несколькими,
у которых энергии активации ниже,
скорость их выше:
CO
+ 1/2O2
= CO2
(катализатор — пары воды)
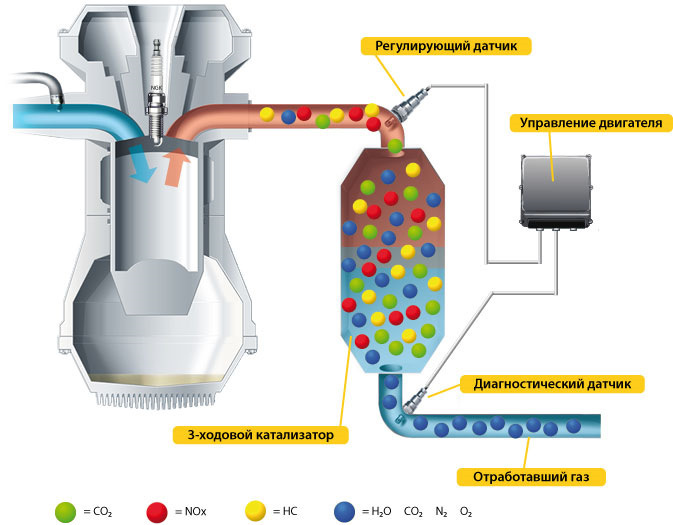
Широкое
применение в химической промышленности
находит гетерогенный катализ. Большая
Большая
часть продукции, вырабатываемой в
настоящее время этой промышленностью,
получается с помощью гетерогенного
катализа. При гетерогенном катализе
реакция протекает на поверхности
катализатора. Отсюда следует, что
активность
катализатора зависит от величины и
свойств его поверхности. Для того чтобы
иметь большую («развитую») поверхность,
катализатор должен обладать
пористой структурой или находиться в
сильно раздробленном (высокодисперсном)
состоянии. При практическом применении
катализатор обычно наносят на носитель,
имеющий пористую структуру (пемза,
асбест и др.).
Как
и в случае гомогенного катализа, при
гетерогенном катализе реакция протекает
через активные промежуточные соединения.
Но здесь эти соединения представляют
собой поверхностные соединения
катализатора с реагирующими веществами.
Проходя через ряд стадий, в которых
участвуют эти промежуточные соединения,
реакция заканчивается образованием
конечных продуктов, а катализатор в
результате не расходуется.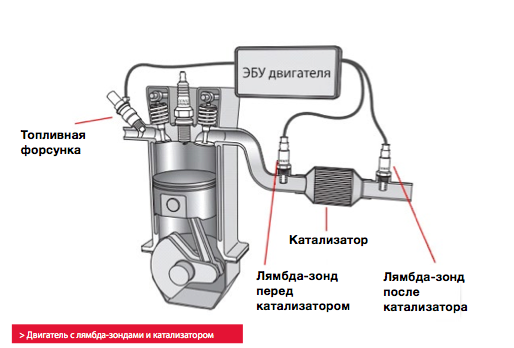
Все
каталитические гетерогенные реакции
включают в себя стадии адсорбции и
десорбции.
Каталитическое
действие поверхности сводится к двум
факторам: увеличение концентрации на
границе раздела и активирование
адсорбированных молекул.
Примеры гетерогенного
катализа:
2H2O
= 2H2O
+ O2
(катализатор – MnO2,)
Н2
+ 1/2 О2
= Н2О
(катализатор — платина)
Очень
большую роль играет катализ в биологических
системах. Большинство химических
реакций, протекающих в пищеварительной
системе, в крови и в клетках животных и
человека, являются каталитическими
.реакциями. Катализаторы, называемые в
этом случае ферментами, представляют
собою простые или сложные белки. Так,
слюна содержит фермент птиалин, который
катализирует превращение крахмала в
сахар. Фермент, имеющийся в желудке, —
пепсин — катализирует расщепление
белков. В организме человека находится
В организме человека находится
около 30 000 различных ферментов: каждый
из них служит эффективным катализатором
соответствующей реакции.
Селективность
действия катализатора – продукты
реакции могут быть разными в зависимости
от того, каким катализатором мы пользуемся.
Резко
замедлить протекание нежелательных
химических процессов в ряде случаев
можно добавляя в реакционную среду
ингибиторы
(явление «отрицательного катализа»).
Влияние катализатора, температуры и растворителя на синтез и выход продукта реакции с виниловым эфиром салициловый кислоты в присутствии винилацетилена
АННОТАЦИЯ
В данной статье исследуется влияние катализатора и температуры на синтез ненасыщенных связывающих сложных эфиров, содержащих винилацетилен и салициловую кислоту. Гидроксиды щелочных металлов были выбраны в качестве высокоосновной среды. Самый высокий из этих результатов наблюдался при выполнении в среде КОН-ДМСО.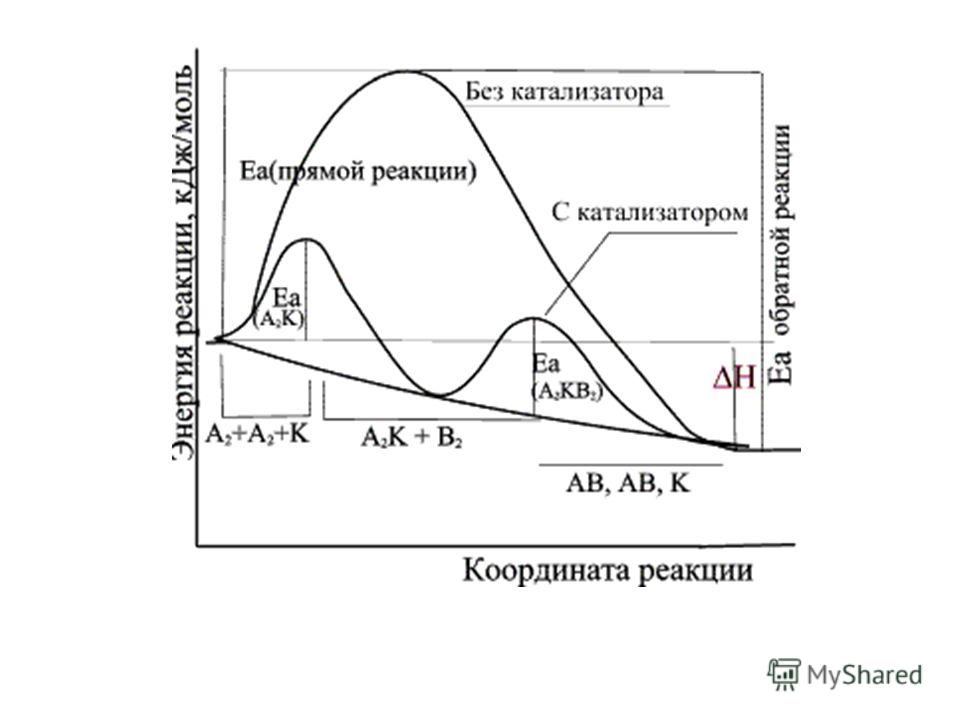 CsF также использовался для улучшения хорошо заземленной среды. Установили, сущность высокой основности системы КОН-ДМСО со слабой сольватацией сильных анионов катионов. Среди катализаторов, использованных в эксперименте, наиболее активным был КОН, при этом салициловая кислота давала 31,8% винилового эфира и 14,5 и 22,7%, соответственно, при использовании LiOH и NaOH.
CsF также использовался для улучшения хорошо заземленной среды. Установили, сущность высокой основности системы КОН-ДМСО со слабой сольватацией сильных анионов катионов. Среди катализаторов, использованных в эксперименте, наиболее активным был КОН, при этом салициловая кислота давала 31,8% винилового эфира и 14,5 и 22,7%, соответственно, при использовании LiOH и NaOH.
ABSTRACT
This article examines the effect of catalyst and temperature on the synthesis of unsaturated binding esters containing vinyl acetylene and salicylic acid. Alkali metal hydroxides were chosen as the highly basic medium. The highest of these results was observed when performed in KOH-DMSO environment. CsF has also been used to improve a well grounded environment. The essence of the high basicity of the KOH-DMSO system with weak solvation of strong cation anions was established. Among the catalysts used in the experiment, KOH was the most active, with salicylic acid giving 31,8% vinyl ester and 14,5 and 22,7%, respectively, when using LiOH and NaOH.
Ключевые слова: ацетилен, винилацетилен, катализатор, салициловая кислота, КОН-ДМСО, диметилформамид, диметилсульфоксид.
Keywords: acetylene, vinyl acetylene, catalyst, salicylic acid, KOH-DMSO, dimethylformamide, dimethyl sulfoxide.
Введение
Ароматические оксикислоты, содержащие винильную группу, отличаются устойчивостью к гидролизу и склонностью к радикальной полимеризации по сравнению с алифатическими аналогами простых виниловых эфиров. Реактивная активность этих веществ как строительных блоков в органическом синтезе очень высока [1,2,4,12,14,17].
В химии синтез арилвиниловых эфиров и их производных быстро развивался за последние несколько десятилетий. Они используются в синтезе новых композитных полимеров, а также в качестве консервантов для растений [1,3,5]. Ацетилен — один из основных сырьевых материалов в химическом синтезе. Это делается за счет треугольника внутри него. Благодаря этим свойствам можно осуществлять синтез очень важных веществ в химической промышленности, а также в синтетической органике [2,3,4,9,11].
Внедрение в химию винилацетилена высокоосновных систем с щелочно-дипольным раствором апротона позволило оптимизировать условия получения трудно синтезируемых виниловых соединений, а также ароматических оксикислот и их виниловых эфиров.
Экспериментальная часть
В ходе исследования систематически изучались реакции винила с винилацетиленом с использованием высокоосновных систем КОН-ДМСО и КОН-ДМФА в присутствии щелочи салициловой кислоты (КОН) [2,5].
Роль ДМСО в системе КОН-ДМСО заключается в том, что под его влиянием происходит диссоциация пары основных ионов, образование низкоосновного аниона димсила с низкой растворимостью:
Следует отметить, что суть этой системы в целом можно объяснить изменениями диэлектрической проницаемости среды, водородными связями и другими эффектами. Введение фторидов металлов в систему ДМСО-КОН увеличивает их основность, упрощает процесс и увеличивает выход виниловых эфиров [1,5,6,8,16].
Для винилсалициловой кислоты использовали каталитическую систему с высоким содержанием оснований CsF-MON-DMSO (M = Li, Na, K). В процессе определено образование винилового эфира салициловой кислоты, схематическое изображение реакции следующее:
В процессе определено образование винилового эфира салициловой кислоты, схематическое изображение реакции следующее:
Изучено влияние природы катализатора на винильный процесс салициловой кислоты. В качестве катализаторов использовали гидроксиды лития, натрия, калия. Во всех случаях обнаружено образование эфира салициловой кислоты. Результаты, полученные в зависимости от природы используемого катализатора, представлены в таблице 1.
Таблица 1.
Влияние салициловой кислоты на выход сложных виниловых эфиров в зависимости от природы катализатора
(продолжительность реакции — 3 часа, температура — 30°C)
|
Катализатор
|
Выход продукта, %
|
|
LiОH
|
14,6
|
|
NаОH
|
22,7
|
|
КОН
|
31,7
|
Согласно результатам, наиболее активным использованным катализатором был КОН, с выходом винилового эфира салициловой кислоты 31,8%, LiOH и NaOH 14,5 и 22,7% соответственно.
Когда эксперименты проводятся без растворителя, процесс получения винилсалициловой кислоты затруднен, так как выход продукта настолько низок, что невозможно было разделить его и определить его состав. Катализатор в количестве 12-24 мас.% Салициловой кислоты испытывали на винил в присутствии ДМСО.
Процесс винилирования проводили при атмосферном давлении в присутствии гидроксидов щелочных металлов. Было установлено, что активность катализатора снижается в следующем порядке:
CsОН . Н2О > КОН . Н2О > NаОН. Н2О >LiОН. Н2О
КОН ва 2КОН*Н2О, КОН*Н2О было показано, что количество воды во всех случаях усложняет виниловый процесс по сравнению с каталитической активностью Было обнаружено, что CsOH относительно высокоэффективен при использовании безводных гидроксидов щелочных металлов в виниловом процессе. Однако дегидратация гидроксидов рубидия и цезия очень затруднена.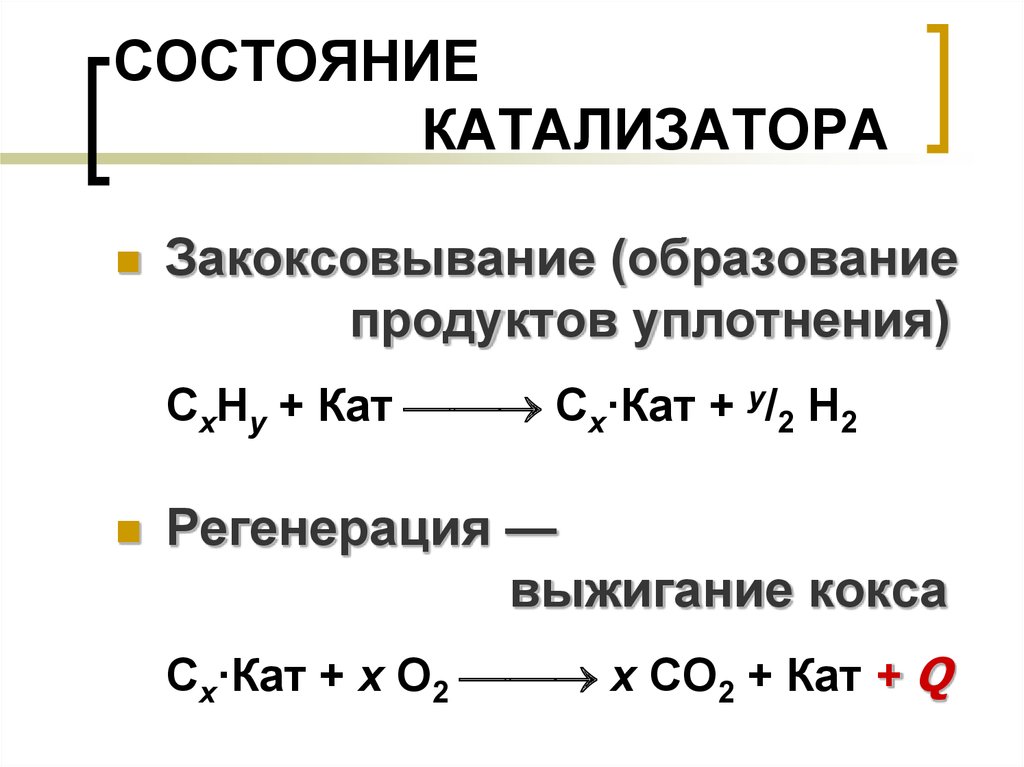 Обычно его кипятят с такими растворителями, как октан, толуол и ксилол, которые образуют азеотропную смесь с водой.
Обычно его кипятят с такими растворителями, как октан, толуол и ксилол, которые образуют азеотропную смесь с водой.
Согласно результатам, полученным в эксперименте, количество КОН в системе оказывает существенное влияние на протекание реакции, и его оптимальное количество составляло 13% по массе салициловой кислоты, в последующих экспериментах количество катализатора проводилось в том же процентном соотношении.
Результаты изучения влияние растворителей на реакцию винилирования салициловой кислоты приведены в табл. 2.
Таблица 2.
Влияние растворителя на виниловый процесс салициловой кислоты (продолжительности реакции 2,5 ч).
|
№
|
Природа растворителя
|
Температура реакции, °C
|
Количество катализатора КОН, % (по отношению к массе салициловой кислоты)
|
Выход винилового эфира салициловой кислоты,%
|
|
1.
|
‑
|
25-30
|
13
|
5,2
|
|
2.
|
ДМСО
|
25-30
|
13
|
20,3
|
|
3.
|
ДМФА
|
25-30
|
13
|
16,3
|
Из приведенных выше данных можно видеть, что природа растворителя оказывает значительное влияние на винильную реакцию салициловой кислоты. В процессе образования винилового эфира салициловой кислоты без растворителя с выходом 5,2%, и в аналогичных условиях в присутствии ДМСО выход составил 20,3%. Для изучения влияния природы растворителя на реакцию процесс проводили в присутствии ДМФА при 25–30°С с содержанием катализатора 11% (по массе резорцина). При этом доходность составила 16,3%. Среди использованных растворителей ДМСО оказался более активным, чем ДМФА в виниловом процессе. Это связано с тем, что, как упоминалось ранее, полярные двухапротонные растворители образуют сильно заземленную систему с КОН. Это увеличивает срок действия КОН и ускоряет нуклеофильное связывание промежуточного соединения — калиевой салициловой кислоты с винилацетиленом.
Для изучения влияния природы растворителя на реакцию процесс проводили в присутствии ДМФА при 25–30°С с содержанием катализатора 11% (по массе резорцина). При этом доходность составила 16,3%. Среди использованных растворителей ДМСО оказался более активным, чем ДМФА в виниловом процессе. Это связано с тем, что, как упоминалось ранее, полярные двухапротонные растворители образуют сильно заземленную систему с КОН. Это увеличивает срок действия КОН и ускоряет нуклеофильное связывание промежуточного соединения — калиевой салициловой кислоты с винилацетиленом.
Для дальнейшего увеличения выхода винилового эфира салициловой кислоты реакцию салициловой кислоты изучали с участием системы КОН-ДМСО-CsF. Температуру поддерживали в диапазоне 25–45°C. Полученные результаты представлены в таблице 3.
Таблица 3.
Влияние температуры на выход салициловой кислоты в виниловом эфире в виниле салициловой кислоты в присутствии системы КОН-ДМСО-CsF
(Количество катализатора КОН по отношению к массе салициловой кислоты — 13%)
|
№
|
Температура реакции,°C
|
Продолжительность реакции, час.
|
Выход винилового эфира салициловой кислоты,%
|
|
1.
|
25-30
|
1
|
25,6
|
|
2.
|
25-30
|
2
|
28,5
|
|
3.
|
25-30
|
3
|
34,2
|
|
4.
|
25-30
|
4
|
35,3
|
|
5.
|
25-30
|
5
|
38,7
|
|
6.
|
30-35
|
5
|
50,2
|
|
7.
|
50-75
|
5
|
36,5
|
Из таблицы видно, что выход винилового эфира салициловой кислоты достигает максимума при увеличении продолжительности реакции с 1 до 5 ч. При температуре 25-30°C и продолжительности реакции 3 часа выход продукта составляет 34,2%. Дальнейшее увеличение продолжительности реакции приводит к снижению выхода винилового эфира салициловой кислоты, его выход достигает максимального значения через 5 часов, т.е. 38,7%. Повышение температуры до 30-35°С привело к увеличению выхода продукта на 50,2%. Повышение температуры выше 50°C привело к снижению выхода продукта. Это можно объяснить олигомеризацией синтезированного винилового соединения и частичным окислением салициловой кислоты и полученного продукта либо снижением растворимости винилацетилена при высоких температурах и деструктивным изменением продукта [7,10,13,15].
Таким образом, исследование винильной реакции салициловой кислоты показало, что ее оптимальными условиями являются: растворитель — ДМСО, количество катализатора КОН — 13% (по отношению к массе резорцина), температура 30-35°С, выход винилового эфира салициловой кислоты составляет 50,2% за 5 часов.
По результатам исследования влияния температуры на протекание винильной реакции салициловой кислоты был также построен график зависимости выхода винилового эфира салициловой кислоты от продолжительности реакции при различных температурах (рис. 1).
Рисунок 1. Влияние продолжительности реакции салициловой кислоты на выход винилового эфира при различных температурах
На основании полученных данных был построен график температурной зависимости выхода продукта (рис. 2). Этот закон объясняется снижением растворимости винилацетилена при высоких температурах, что приводит к уменьшению его содержания в реакционной системе, скорости реакции и выхода винилового эфира в моносостоянии резорцина.
Рисунок 2. Температурная зависимость выхода винилового эфира салициловой кислоты (продолжительность реакции 5 часов)
Заключение: По результатам экспериментов было установлено, что температура оказывает существенное влияние на выход продукта. Во всех случаях выход продукта увеличивается в зависимости от времени и температуры. При повышении температуры с 30 до 35°C при продолжительности реакции 5 ч выход продукта также увеличивается с 38,7 до 50,2% соответственно. Дальнейшее повышение температуры относительно медленно замедляет реакцию, и при 75°C выход составляет 36,5%.
Были изучены эффекты катализатора, температуры и растворителя на виниловую реакцию на основе винилацетилена.
Список литературы:
- Трофимов Б.А., Нестеренко Р.Н., Михалева А.И. Новые примеры винилирования NH-гетероциклов ацетиленом в системе КОН-ДМСО // ХГС. -Рига, 1986. -№4. -С.481-485.

- Trofimov, B. A., Oparina, L. A., Kolyvanov, N. A., Vysotskaya, O. V., &Gusarova, N. K. Nucleophilic addition to acetylenes in superbasic catalytic systems: XVIII. Vinylation of phenols and naphthols with acetylene //Russian Journal of Organic Chemistry. – 2015. – Т. 51. – №. 2. – С. 188-194.
- Трофимов Б.А. Суперосновные среды в химии ацетилена //ЖОрХ-Ленинград, 1986. -Т.ХХII. -вып.9, -С.1991-2011.
- Mирхамитова Д.Х., Нурманов С.Э., Хабиев Ф.М., Худайберганова С.З., Teшабаев Б. Разработка катализаторов для синтез N-винилморфолина. // II Межд. науч. конф. «Современная химия: Успехи и достижения». -Чита. -2016 г. -C. 282-283.
- Зиядуллаев О.Э., Мирхамитова Д.Х., Нурманов С.Э. Турли усуллар ёрдамида ароматик ацетилен спиртлари синтези. // ЎзМУ Хабарлари журнали. -Тошкент, -2012. -№3/1. -С.25-29.
- Мирхамитова Д.Х., Нурманов С.Э., Жураев В.Н. Каталитический синтез N-винилпиперидина. // Журн. ХПС. -Ташкент. -2001. -Спец.
 вып. -С.86-87.
вып. -С.86-87. - Мирхамитова Д.Х. Азот тутган гетероҳалқали бирикмаларни винилҳосилалари синтези ва хоссалари. // ЎзМУ Хабарлари журнали. -Ташкент, -2012. -№3/1. -С.79-84.
- М.С. Рахматов ., С.Э. Нурмонов., В.Н. Ахмедов. Ароматик оксикислоталар винил эфирлари синтези. “Замонавий ишлаб чикаришнинг мухандислик ва технологик муаммоларини инновацион ечимлари” Халкаро илмий анжуман материаллари Бухоро. 2019. 93-94 б.
- B.B. Olimov, V.N. Ahmedov, S. Hayitov. Ikki atomli fenollar asosida vinilli efirlarni olish usullari. Fan va texnologiyаlar taraqqiyoti ilmiy – texnikaviy jurnal. — № 1/2020.
- Б.Б. Олимов, В.Н. Ахмедов, Ш.К. Назаров. Электронная структура и квантово-химические расчёты виниловых эфиров фенолов. U55 Universum: химия и биология: научный журнал. – № 4(70). М., Изд. «МЦНО», 2020. – 53-57с.
- Nazarov Shomurod Komilovich, Olimov Bobur Bahodirovich, Akhmedov Vohid Nizomovich. Еlectronic structure and quantum-chemical calculations of vinyl esters of phenols.
 Austrian Journal of Technical and Natural Sciences
Austrian Journal of Technical and Natural Sciences
Scientifi journal № 3–4 2020 (March – April). - В.Н. Ахмедов, Б.Б. Олимов. Винилацетилен асосида фенолларнинг винил эфирлари синтези. “Замонавий ишлаб чиқаришда муҳандислик ва технологик муаммоларнинг инновацион ечимлари” халқаро илмий анжуман материаллари. 3 ТОМ, 14-16 ноября 2019 г. Бухара-2019.
- В.Н. Ахмедов, Б.Б. Олимов. Способ получения виниловых эфиров на основе винилацетилена. Gaydar Aliyevning 97 yilligiga bag’ishlangan IV yosh tadqiqotchilarning xalqaro ilmiy anjumani. 2020 yil, Boku muhandislik universiteti, Xirdalan / Ozarbayjon.
- Мирхамитова Д.Х., Нурманов С.Э., Тиллабаев А.А., Сирлибаев Т.С. Гомогенно-каталитический синтез N-виниланабазина. // журн. Вестник ГулГУ. -Гулистан. -2003. -№4. -С.86-88.
- С.Абдувалиева, С.Э.Нурманов, Д.Х.Мирхамитова, Б.Р.Абдурасулов. Юқори асосли системада бензотриазолни виниллаш. // “Биоорганик кимё фани муаммолари” Республика конференцияси.
 -Наманган. 21-22 ноябр 2014, -С.286-288.
-Наманган. 21-22 ноябр 2014, -С.286-288. - Mirkhаmitоvа D.Kh., Nurmаnоv S.E., Khudаybеrgаnоvа S.Z., Yodgorova M. Catalytic vinylation of some heterocyclic amines at the atmospheric pressure. // Межд. конф. «Актуальные проблемы инновационных технологий в развитии химической нефтегазовой и пищевой промышленности». -Ташкент. 26 мая 2016 г. -С.84-85.
- С.Б.Абдувалиева, Д.Х.Мирхамитова, С.Э.Нурманов. Бензотриазолни гомоген-каталитик виниллаш. // Материалы VIII Межд. научно-технической конф. “Актуальные проблемы химии и химической технологии”, -Навои. 19-21 ноября 2015 г. -С.80.
The Catalyst Effect — Эффект катализатора
Лидерство не зависит от титула или авторитета. Речь идет о том, чтобы сделать всех вокруг вас лучше.
Слишком многие лидеры не знают, как развивать своих людей
или просто не знают, с чего начать, что приводит к:
Начать
Ваша организация может стать катализатором на любом уровне.

Мы поможем вам это осуществить.
Слишком многие лидеры не знают, как развивать своих людей, или просто не знают, с чего начать. Мы поможем вам определить конкретные рычаги для вовлечения сотрудников, создания более сильных команд и стимулирования роста.
Наши инструкторы сертифицированы для предоставления индивидуального дизайна лидерства и фасилитации. Мы создадим вашу дорожную карту для развития каталитического лидерства на всех уровнях вашей организации.
Инвестируйте в данные, которые помогут вам стать катализатором. Мы сочетаем наши основанные на исследованиях, проверенные основные опросы с передовыми инструментами и платформами для индивидуального подхода к мощным позитивным изменениям.
«Эффект Катализатора» прямо указывает на то, что нужно, чтобы стать настоящим лидером, благодаря коллективному доверию и наделению полномочиями. Когда кто-то решает отказаться от своей личной победы ради прогресса команды, результаты становятся мощными и реальными».
Стивен М. Кови
Автор бестселлера СКОРОСТЬ доверия: единственное, что меняет все
«У лучших лидеров и коллег есть нечто общее: они делают всех вокруг себя лучше. Это практическое руководство по развитию этой способности в вашей команде».
Адам Грант
Автор бестселлеров New York Times ДАВАЙ И ВЗИМАЙ, ОРИГИНАЛЫ, и ВАРИАНТ B с Шерил Сандберг
«Эффект Катализатора освещает путь для каждого человека в каждой организации, чтобы увидеть себя в качестве лидеров. Это показывает нам, что каждый является лидером и может лучше руководить, если признает эту истину».
Анжела Дакворт
автор бестселлера GRIT
Начните развивать свою команду
всего за три простых шага.
Z
Мы обсудим ваши потребности, организационную стратегию, основные препятствия и предоставим вам обзор того, как мы помогли компаниям процветать.
Z
Мы разработаем для вас индивидуальный план действий с расставленными приоритетами, чтобы выявить конкретные рычаги для вовлечения сотрудников, создания более сильных команд и стимулирования роста.
Z
Используя нашу индивидуальную структуру, мы будем сотрудничать вместе, чтобы согласовать видение вашей компании и кадровую стратегию. Когда все удовлетворены и работают, организации растут.
Каждый может изменить правила игры, если у него есть инструменты для роста.
Мы знаем, что вы хотите, чтобы каждый в вашей организации каждый день приносил пользу. Для этого вам нужна стратегия развития ваших людей. Проблема в том, что в прошлом вы испробовали множество подходов, которые не сработали. Вы знаете, что вам нужен отличный фреймворк, но не знаете, с чего начать, из-за чего чувствуете разочарование и подавленность.
Как бывшие руководители организаций и топ-менеджеры отдела кадров, мы были там, где вы находитесь сегодня. Мы понимаем, как вы себя чувствуете, поэтому мы использовали этот опыт, наряду с обширными исследованиями, для создания концепции эффекта катализатора, чтобы помочь таким же лидерам, как и вы.
Мы готовы помочь вам начать развивать своих людей и создать команду каталитических лидеров! Давайте начнем!
Сделайте всех вокруг себя лучше!
Мы помогаем каждому стать лидером, где бы он ни находился.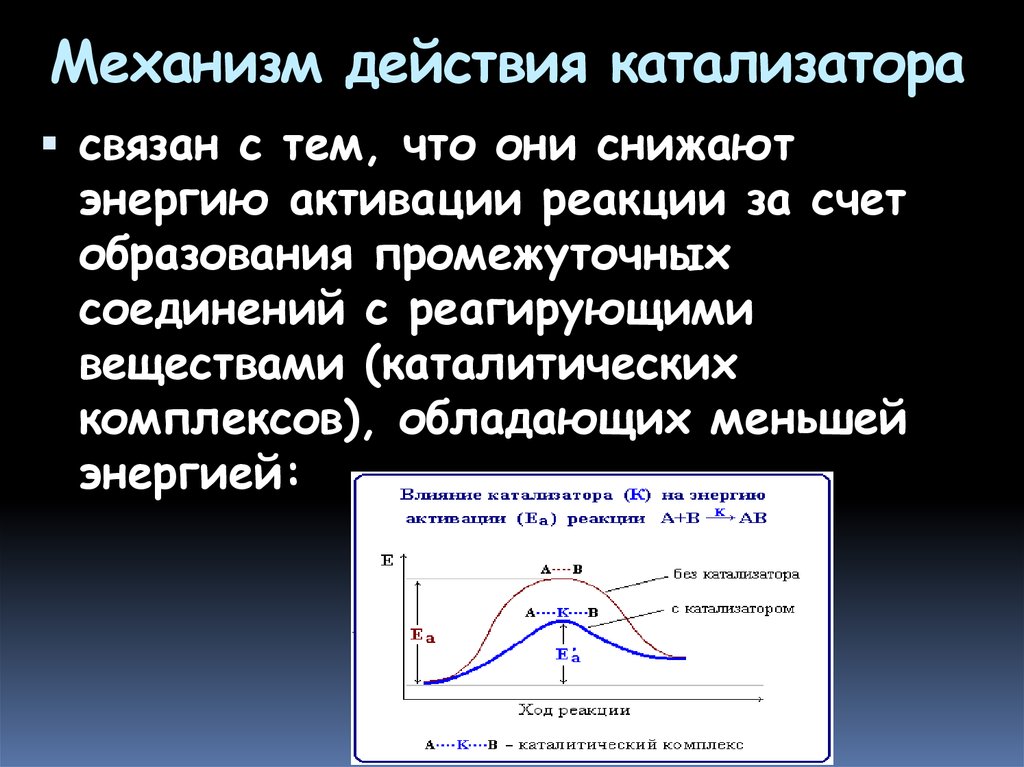
Мы переходим к вопросу о том, что влияет на производительность команды.
Когда все удовлетворены и работают, организации растут.
Книга — Эффект катализатора
КНИГА
12 навыков и поведенческих моделей, которые помогут повысить вашу результативность и эффективность команды
Купить на Amazon
Джерри Тумер, Крейг Колдуэлл, Стив Вейценкорн, Челси Кларк
03
03 Обложка
Знакомы ли вы с коллегами, которые в ту минуту, когда они входят в конференц-зал, на сцену или на игровое поле, поднимают настроение вокруг себя? Кто-то, чье влияние в команде было видно почти во всем, что было сказано и сделано.
Эти люди являются катализаторами — они способствуют совершенствованию поведения и производительности всей команды.
Эффект Катализатора определяет поведение и навыки, необходимые для лидерства, где бы вы ни находились, независимо от вашей роли или должности. В нем описываются мощные принципы лидерства и командной работы, которые повысят производительность отдельных лиц, команд и всей вашей организации.
Это необходимое руководство покажет вам, как научиться и применять на практике эти каталитические компетенции и помочь вашей группе и организации добиться большего успеха, улучшить командную динамику и помочь товарищам по команде вырасти в статусе, увеличивая их ценность.
КУПИТЬ НА AMAZON
УЧИТЬСЯ В РЕАЛЬНОМ РЕЖИМЕ
Похвалы за книгу
«Эта замечательная новая книга «Эффект катализатора» расскажет о том, что нужно, чтобы стать настоящим лидером благодаря коллективному доверию и наделению полномочиями. . Когда кто-то решает отказаться от своей личной победы ради прогресса команды, результаты являются мощными и реальными. Эта книга покажет вам, как это сделать. Великолепно вдохновляющее чтение!»
Стивен М. Р. Кови
The New York Times и № 1 Wall Street Journal автор бестселлеров СКОРОСТЬ доверия и соавтор книги Smart Trust
«[Эффект катализатора] имеет отношение ко многим аспектам жизни; работа, спортивные команды, волонтерские группы и т. д. Мало того, что идея этой книги нова и уникальна, но и то, как в книге представлены примеры из реальной жизни, которые я могу понять, сделало ее интересной и увлекательной. Он содержит информацию о том, «что» и «как», чтобы помочь читателю стать катализатором для людей и групп, с которыми он работает. Отличная и важная книга!»
д. Мало того, что идея этой книги нова и уникальна, но и то, как в книге представлены примеры из реальной жизни, которые я могу понять, сделало ее интересной и увлекательной. Он содержит информацию о том, «что» и «как», чтобы помочь читателю стать катализатором для людей и групп, с которыми он работает. Отличная и важная книга!»
Бетти Эллисон
Amazon Review
«Книга [Эффект катализатора] и концепция лидерства действительно произвели фурор среди моих сотрудников. В моей организации около 50 сотрудников, и многие из них только начинают свою профессиональную карьеру. Несмотря на то, что они молоды, мне нужно, чтобы они все вели с того места, где они есть, и считали себя лидерами. Эффект катализатора помогает нам изменить этот аспект нашей культуры».
К.Дж. Абернати
Обзор Amazon
Превосходное, краткое чтение для людей любого возраста, ищущих творческие идеи и возможности для повышения своего влияния в своей компании или организации.
Gayle Kaye
Amazon Review
«Высокоэффективные организации, будь то коммерческие, некоммерческие, религиозные или государственные, имеют общий «секретный соус» или «катализатор» успеха: превосходство в командной работе. Преобразующие, ориентированные на ценность и результаты организации, ориентированные на потребителя, признают, что лидерство и командная работа синтезируются или «сплавляются» вместе, что приводит к общему стратегическому видению и оперативной реализации. «Эффект катализатора» — это книга, основанная на исследованиях, которая определяет «секретный соус» и представляет собой простую для понимания дорожную карту для достижения успеха. Я очень рекомендую эту книгу для всех. Вы часть команды, и мы все хотим, чтобы наша домашняя команда победила!»
Достопочтенный доктор Стивен Л. Джонсон
11-й администратор Агентства по охране окружающей среды США
«Мне очень нравятся идеи, изложенные в книге. Тщательно проработанный и полный практических советов, «Эффект катализатора» освещает путь для каждого человека в каждой организации, чтобы увидеть себя в качестве лидеров.



 вып. -С.86-87.
вып. -С.86-87. Austrian Journal of Technical and Natural Sciences
Austrian Journal of Technical and Natural Sciences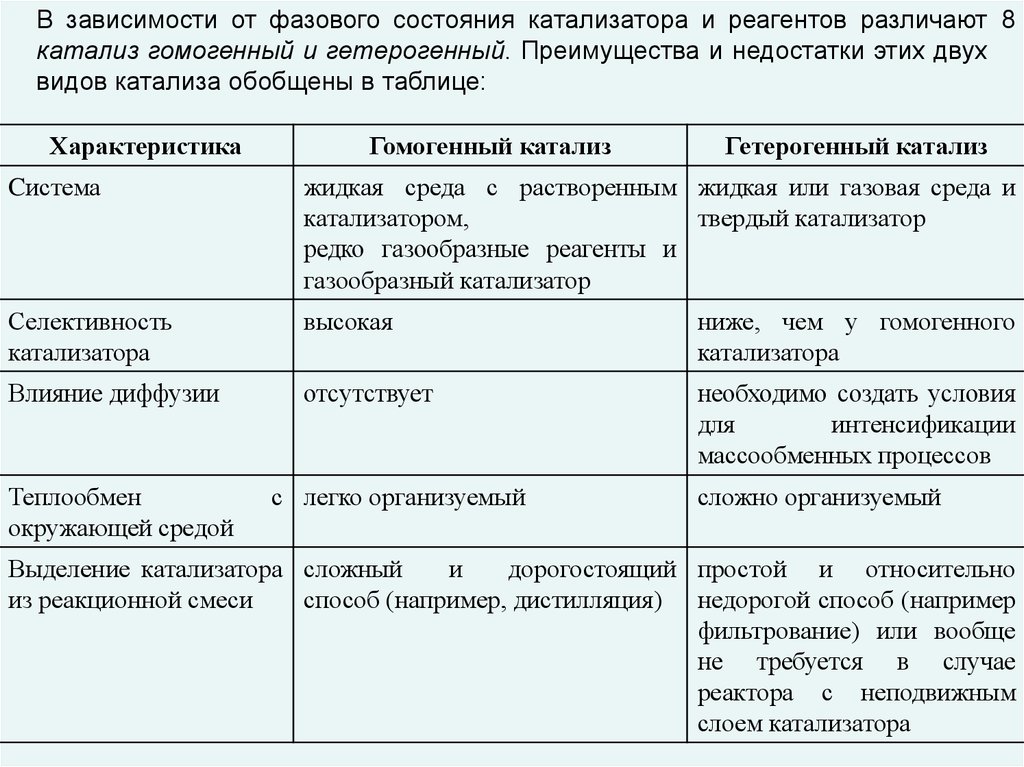 -Наманган. 21-22 ноябр 2014, -С.286-288.
-Наманган. 21-22 ноябр 2014, -С.286-288.